به گزارش ایسنا و به نقل از وبسایت رسمی "دانشگاه ایالتی آریزونا"(ASU)، بررسی جدید پژوهشگران آمریکایی، به معرفی برخی از سرنخهای مولکولی دقیقی میپردازد که با یکی از علل اصلی مرگ و ناتوانی مرتبط هستند. این سرنخهای مولکولی، عامل وضعیتی هستند که به عنوان "آسیب مغزی تروماتیک"(TBI) شناخته میشود.
آسیب مغزی تروماتیک، یک نگرانی رو به رشد برای سلامت عمومی است که بیش از ۱.۷ میلیون آمریکایی را تحت تأثیر قرار میدهد و هزینه سالانه آن تا ۷۶.۵ میلیارد دلار تخمین زده میشود. این بیماری، یکی از علل اصلی مرگ و میر و ناتوانی کودکان و بزرگسالان جوان در کشورهای صنعتی است و افرادی که آن را تجربه میکنند، احتمال بیشتری دارد که به نقصهای شناختی و رفتاری شدید و بلندمدت دچار شوند.
"سارا استابنفلد"(Sarah Stabenfeldt)، استاد دانشگاه ایالتی آریزونا و سرپرست این پژوهش گفت: مکانیسمهای مولکولی و سلولی عامل پیشروی آسیب مغزی تروماتیک، چند وجهی هستند و هنوز به طور کامل شناسایی نشدهاند. این پیچیدگی، بر توسعه گزینههای تشخیصی و درمانی تأثیر میگذارد. هدف پژوهش ما، پرداختن به این محدودیتها است.
رویکرد پژوهشی استابنفلد و گروهش، انجام دادن یک جستجو برای آشکار کردن چندین امضای مولکولی کلیدی به نام نشانگرهای زیستی که بلافاصله پس از آسیب شناسایی میشوند و همچنین، تشخیص پیامدهای بلندمدت آسیب مغزی تروماتیک است.
استابنفلد ادامه داد: آسیبشناسی مربوط به آسیب مغزی تروماتیک به مرور زمان تکامل مییابد و تغییر میکند. این بدان معناست که یک پروتئین یا گیرنده ممکن است طی یک مرحله از آسیب تنظیم شود. این محیط پویا، توسعه یک راهبرد موفق را پیچیده میکند.
پژوهشگران برای غلبه بر این محدودیتها، از یک مدل موش برای پژوهش خود استفاده کردند تا با شناسایی نشانگرهای زیستی منحصربهفرد که در پی یک آسیب یا بیماری آشکار میشوند، به بررسی علل ریشهای آسیب مغزی تروماتیک بپردازند.
استابنفلد گفت: ترومای عصبی، یک زمینه تثبیتشده است که مدلهای حیوانی پیشبالینی را برای درک بهتر آسیبشناسی مربوط به آسیب مغزی تروماتیک و ارزیابی اثربخشی مداخلات درمانی ایجاد و مشخص کرده است. استفاده از یک مدل تثبیتشده موش، ما را قادر ساخت تا نشانگرهای زیستی را کشف کنیم که نشان میدهند پیچیدگی و تکامل آسیبشناسی در کجا پیشروی میکند.
دانشمندان اغلب میتوانند طراحی عوامل درمانی یا دستگاههای تشخیصی را براساس کشف نشانگرهای زیستی آغاز کنند. استابنفلد و گروهش، از یک روش "از پایین به بالا" برای کشف نشانگرهای زیستی استفاده کردند.
"برایانا مارتینز"(Briana Martinez)، پژوهشگر ارشد این پروژه گفت: روشهای کشف از بالا به پایین، بر ارزیابی نشانگرهای زیستی براساس مشارکت آنها در بیماری متمرکز هستند. در مقابل، یک روش از پایین به بالا، تغییرات رخداده در ترکیب بافت را تجزیه و تحلیل میکند و به دنبال راهی برای ارتباط این تغییرات با بیماری میگردد. این یک روش بیطرفانهتر است اما میتواند مخاطرهآمیز باشد زیرا ممکن است نشانگرهایی شناسایی شوند که مختص بیماری یا آسیبشناسی مورد نظر نیستند.
سپس پژوهشگران، از چندین دستگاه و روش پیشرفته برای شناسایی و بررسی مولکولها استفاده کردند؛ از جمله روش موسوم به "طعمه" برای صید مولکولهای مورد نظر، توالییابی DNA برای شناسایی اهداف پروتئینی در ژنوم و طیفسنجهای جرمی برای تعیین توالی قطعات پپتید.
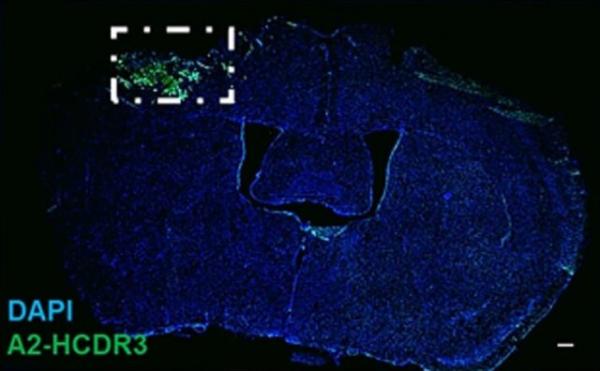
یکی دیگر از موانع اکتشاف، فیزیولوژی منحصربهفرد سد خونی مغز است که برای محافظت از مغز در برابر آسیب یا مواد شیمیایی مضر کار میکند.
استابنفلد گفت: سد خونی مغز، سدی بین عروق و بافت مغز است. سد خونی مغز در یک شخص سالم، تبادل مواد مغذی و مواد زائد را از خون به مغز و بالعکس تنظیم میکند و مغز و سیستم عصبی مرکزی را بخشبندی میکند. در هر حال، این مانع میتواند انتقال دارو به مغز را نیز پیچیده کند؛ به طوری که بیشتر مولکولها و داروها نتوانند به طور غیر فعال از این مانع عبور کنند. بنابراین، زمینه تحویل دارو به دنبال راههایی برای تعدیل مکانیسمهای ورود و رسیدن دارو بوده است.
هنگامی که آسیب مغزی تروماتیک رخ میدهد، آسیب اولیه میتواند سد خونی مغز را مختل کند که باعث ایجاد مرگ سلولی و از هم گسیختن بافتها و مواد باقیمانده میشود.
آسیب بلندمدت باعث التهاب و تورم میشود و همچنین میتواند اختلال در منابع انرژی مغز را به همراه داشته باشد، جریان خون به مغز را مختل کند و به افزایش مرگ سلولهای عصبی و ناتوانی دائمی منجر شود.
مزیت مهم مجموعه دستگاهها و روشهای آزمایشی استابنفلد و گروهش این است که مولکولها و نشانگرهای زیستی شناساییشده آنقدر کوچک هستند تا از سوراخهای ریز درون شبکه سد خونی مغز بلغزند و راه را برای درمان مبتنی بر مولکولها هموار کنند.
بنابراین میتوان گفت که این گروه پژوهشی به رغم وجود چنین موانعی، راهحلی یافتهاند. این گروه پژوهشی، مجموعهای از نشانگرهای زیستی منحصربهفرد را یافتند که فقط با مراحل حاد یا مزمن آسیب مغزی تروماتیک مرتبط هستند.
مارتینز گفت: روش ما برای کشف نشانگر زیستی به اندازه کافی حساس بود تا بتواند آسیب مغزی را که نمونههای آن در آزمایشهای مختلف جمعآوری شده بودند، تشخیص دهد. واقعا جالب بود که میدیدیم پروتئینهای دخیل در بیماریهای عصبی، طی هفت روز پس از آسیب تشخیص داده شدند. مشاهده این تفاوتها نشان میدهد که این روش چقدر میتواند در کشف جنبههای مختلف آسیب مغزی سودمند باشد.
همچنین، این روش ممکن است توضیح دهد که چرا افرادی که به آسیب مغزی تروماتیک مبتلا هستند، بیشتر در معرض ابتلا به بیماریهای تخریبکننده عصبی مانند پارکینسون و آلزایمر قرار میگیرند.
این کشف موفق، به عنوان پایهای برای نسل بعدی درمان و تشخیص هدفمند آسیب مغزی تروماتیک عمل خواهد کرد.
این پژوهش، در مجله "Science Advances" به چاپ رسید.
- 9
- 4