به گزارش ایسنا به نقل از ساینس دیلی، درد ممکن است ناخوشایند باشد، اما در بیشتر موارد یک نقش حیاتی و حتی نجاتبخش دارد. دردهای کوتاهمدت مانند سیگنالهای هشداردهنده هستند که از ما در برابر آسیب محافظت میکنند. وقتی یک ماهیتابه داغ را لمس میکنید و انگشت پایتان یا سرتان به جایی برخورد میکند، سیستم عصبی شما فوراً یک هشدار میفرستد که شما را وادار میکند تا پیش از بروز آسیب بیشتر، خودتان را عقب بکشید. درد از بین میرود، بدن بهبود مییابد و شما به یاد میآورید که دفعه بعد چه کاری را نباید انجام دهید.
داستان درد مزمن کاملاً متفاوت است. در این شرایط، سیگنال هشدار حتی پس از بهبود آسیب هم متوقف نمیشود. درد مزمن به یک همراه دائمی و نامرئی تبدیل میشود که میتواند سالها یا حتی دههها ادامه یابد. «نیکلاس بتلی»(Nicholas Betley)، متخصص علوم اعصاب «دانشگاه پنسیلوانیا»(UPenn) گفت: این تنها یک آسیب نیست که بهبود نمییابد، بلکه یک ورودی مغزی است که حساس و بیشفعال شده است و تعیین چگونگی آرام کردن آن ورودی میتواند به ارائه درمانهای بهتر کمک کند.
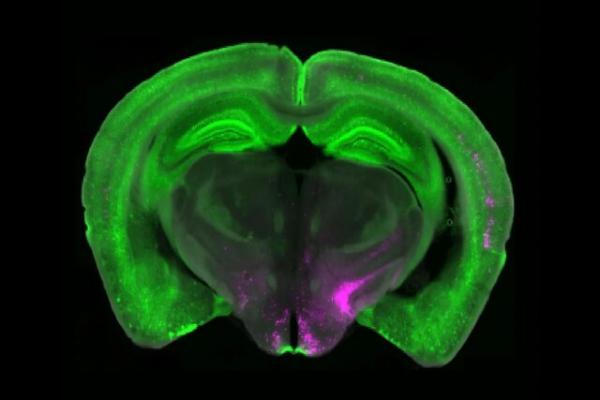
بتلی به همراه پژوهشگران «دانشگاه پیتسبرگ»(University of Pittsburgh) و «مؤسسه پژوهشی اسکریپس»(Scripps Research Institute)، قطعه مهمی را از پازل درد مزمن کشف کردهاند. تحقیقات آنها به گروه خاصی از سلولهای بنیادین مغز به نام «نورونهای بیانکننده گیرنده»(Y1R) اشاره دارد که در «هسته پارابراکیال»(Parabrachial nucleus) مغز قرار گرفتهاند. این نورونها در حالتهای درد مداوم فعال میشوند، اما سیگنالهای مربوط به گرسنگی، ترس و تشنگی را نیز پردازش میکنند. این نشان میدهد که مغز میتواند واکنش به درد را در زمان نیازهای فوریتر تنظیم کند.
یافتههای این پژوهش نشان میدهند که تسکین درد ممکن است امکانپذیر باشد، زیرا همان طور که پژوهشگران در مقاله خود نوشتهاند، مدارهایی در مغز وجود دارند که میتوانند فعالیت نورونهای انتقالدهنده سیگنال درد را کاهش دهند.
ردیابی درد در مغز
گروه بتلی با همکاری پژوهشگران «آزمایشگاه تیلور»(Taylor lab) در دانشگاه پیتسبرگ، از تصویربرداری کلسیم برای به تصویر کشیدن در لحظه فعالیت نورونها در مدلهای حیوانی درد کوتاهمدت و بلندمدت استفاده کردند. آنها دریافتند که نورونهای Y1R صرفاً به حملات سریع درد واکنش نشان نمیدهند، بلکه در طول درد بلندمدت به طور پیوسته فعال میشوند. این پدیده به عنوان «فعالیت تونیک»(Tonic activity) شناخته میشود.
بتلی این پدیده را با موتوری که حتی پس از پارک کردن ماشین روشن مانده است، مقایسه میکند. سیگنالهای درد حتی زمانی که بهبودی جسمی کامل به نظر میرسد، همچنان در پسزمینه به صدا در میآیند. این فعالیت عصبی مداوم ممکن است توضیح دهد که چرا برخی افراد مدتها پس از آسیب یا جراحی همچنان احساس درد میکنند.
این پژوهش از یک کشف غیرمنتظره که بتلی پس از پیوستن به دانشگاه پنسیلوانیا در سال ۲۰۱۵ به آن رسیده بود، سرچشمه گرفت. کشف او این بود که به نظر میرسد گرسنگی، درد مزمن را کاهش میدهد. بتلی گفت: با توجه به تجربه خودم احساس کردم وقتی واقعاً گرسنه هستیم، تقریباً هر کاری را برای به دست آوردن غذا انجام میدهیم. وقتی صحبت از درد مزمن و بلندمدت به میان میآید، به نظر میرسد گرسنگی در کاهش درد از داروی مسکن «ادویل»(Advil) قویتر است.
این اطلاعات، الهامبخش تحقیقات بیشتر شدند. «نیتسان گلدشتاین»(Nitsan Goldstein)، دانشجوی سابق کارشناسی ارشد دانشگاه پنسیلوانیا دریافت که سایر حالتهای حیاتی بقا مانند تشنگی و ترس نیز میتوانند درد بلندمدت را سرکوب کنند. این گروه پژوهشی با همکاری «آزمایشگاه کندی»(Kennedy lab) در مؤسسه پژوهشی اسکریپس نشان دادند که وقتی بقای فوری در اولویت قرار میگیرد، هسته پارابراکیال مغز میتواند ورودیهای حسی را نسبت به درد آرام فیلتر کند.
گلدشتاین گفت: این به ما نشان داد که مغز احتمالا یک روش ذاتی را برای اولویتبندی نیازهای فوری بقا بر درد دارد و ما میخواستیم نورونهای مسؤول این تغییر را پیدا کنیم.
بخش کلیدی این تغییر، یک مولکول سیگنالدهنده موسوم به «نوروپپتید Y» یا «NPY» است که به مغز کمک میکند تا به مدیریت نیازهای رقابتی بپردازد. وقتی گرسنگی یا ترس اولویت پیدا میکنند، NPY بر گیرندههای Y1 در هسته پارابراکیال تأثیر میگذارد تا سیگنالهای درد مداوم را تعدیل کند.
گلدشتاین توضیح میدهد: انگار مغز این کلید داخلی را دارد که درد را نادیده بگیرد. اگر گرسنه باشید یا با یک شکارچی روبهرو شوید، نمیتوانید تحمل کنید که درد بلندمدت شما را از پا درآورد. نورونهایی که توسط تهدیدهای دیگر مانند این نمونهها فعال میشوند، NPY منتشر میکنند و NPY نیز سیگنال درد را خاموش میکند تا سایر نیازهای بقا در اولویت قرار بگیرند.
یک سیگنال پراکنده
پژوهشگران در این پروژه، هویت مولکولی و آناتومیکی نورونهای Y1R را در هسته پارابراکیال مشخص کردند. آنها دریافتند که نورونهای Y1R، دو جمعیت آناتومیکی یا مولکولی منظم را تشکیل نمیدهند. در عوض، این نورونها در بسیاری از انواع سلولهای دیگر پراکنده شدهاند.
بتلی گفت: این مانند نگاه کردن به خودروها در یک پارکینگ است. ما انتظار داشتیم همه نورونهای Y1R به صورت خوشهای از خودروهای زرد باشند که در کنار یکدیگر پارک شدهاند، اما در اینجا نورونهای Y1R مانند رنگ زردی هستند که در میان خودروهای قرمز، آبی و سبز پراکنده شدهاند. ما دقیقاً نمیدانیم چرا، اما فکر میکنیم این توزیع پراکنده ممکن است به مغز امکان دهد تا انواع گوناگون ورودیهای دردناک را در مدارهای متعدد تعدیل کند.
به گفته بتلی، چیزی که او را درباره این کشف هیجانزده میکند، بررسی بیشتر پتانسیل آن برای استفاده از فعالیت عصبی Y1 به عنوان نشانگر زیستی درد مزمن است؛ چیزی که توسعهدهندگان دارو و پزشکان مدتهاست آن را نداشتهاند.
بتلی ادامه داد: بیماران در حال حاضر ممکن است به متخصص ارتوپد یا مغز و اعصاب مراجعه کنند و هیچ آسیب آشکاری در آنها وجود نداشته باشد، اما بیماران هنوز درد دارند. چیزی که ما در این پژوهش نشان دادهایم، این است که امکان دارد مشکل در اعصاب محل آسیب نباشد، بلکه در خود مدار مغز باشد. اگر بتوانیم این نورونها را هدف قرار دهیم، مسیر کاملاً جدیدی برای درمان باز میشود.
همچنین، این پژوهش نشان میدهد که مداخلات رفتاری مانند ورزش، مدیتیشن و درمان شناختی رفتار ممکن است بر نحوه فعالیت این مدارهای مغزی تأثیر بگذارند؛ درست همان طور که گرسنگی و ترس در آزمایشگاه این کار را انجام دادند.
بتلی گفت: ما نشان دادهایم که این مدار انعطافپذیر است و میتوان آن را بالا یا پایین برد. بنابراین، آینده فقط طراحی یک قرص نیست، بلکه پرسش این است که چگونه رفتار، آموزش و سبک زندگی میتواند نحوه رمزگذاری درد توسط این نورونها را تغییر دهد.
این پژوهش در مجله «Nature» به چاپ رسید.
- 18
- 3